เครื่องระเหยสารสุญญากาศ
เทคนิคการทำระเหยแบบหมุน กับขั้นตอนการกลั่น
ขั้นตอนการกลั่นจะใช้เพื่อนำสารละลายที่เป็นไอได้ ออกจากสารผสมของเหลวผ่านการระเหยและการควบแน่นตามลำดับ ในห้องปฏิบัติการ นักเคมีและนักชีววิทยามักจะใช้การกลั่นและการทำระเหยแบบหมุน
ประวัติของการกลั่น
การพัฒนาที่ผ่านมาของการทำระเหยแบบหมุน หรือ «การแยกแบบหยดต่อหยด» เริ่มใช้กันตั้งแต่หลายพันปีที่ผ่านมา ประวัติมากมายเกี่ยวกับขั้นตอนการกลั่นที่วิวัฒนาการมาตามกาลเวลาจะแสดงไว้ในตารางด้านล่าง
| 3,500 BC | ชาวเปอร์เชียคิดค้นการกลั่นเพื่อผลิตน้ำกุหลาบ เทคนิคการกลั่นนั้นแพร่หลายอย่างรวดเร็วไปทั่วยุโรป แอฟริกาเหนือ และเอเชีย ขั้นตอนการกลั่นนั้นนำมาใช้เพื่อผลิตสารสกัด น้ำทะเลที่แยกเกลือออกได้ และในการทำแร่แปรธาตุ |
| ศตวรรษที่ 2 | เมื่อศาสนาและศาสตร์เคมีเติบโตขึ้น รวมถึงความนิยมในการทำแร่แปรธาตุ จึงทำให้เกิดการค้นหา “the prima materia หรือสารตั้งต้นจักรวาล” ซึ่งเป็นวัสดุตั้งต้นพื้นฐานที่ไม่มีคุณภาพหรือความหนาแน่นจำเพาะ นักแร่แปรธาตุต่างแสวงหาวิธีการทางเคมีเพื่อแปรวัสดุธรรมชาติให้ได้วัสดุพื้นฐานแล้วจึงนำวัสดุพื้นฐานมาทำให้เกิดเป็นรูปแบบที่ต้องการ เช่น ทองคำ ในการทดลองนั้น เกิดการค้นพบองค์ประกอบทางเคมีมากมาย การพัฒนาขั้นตอนและเครื่องมือที่มีอยู่ ไปจนถึงการค้นพบวิธีใหม่ๆ ที่ยังคงใช้กันในศาสตร์ทางเคมีสมัยใหม่จนถึงปัจจุบันนี้ รวมไปถึงการค้นพบเทคโนโลยีการกลั่นที่ใช้มาจนถึงทุกวันนี้ จากจุดเริ่มต้นที่เป็นเพียงแค่การออกแบบเท่านั้น องค์ประกอบมาตรฐานทั้งสี่ของอุปกรณ์การกลั่นนี้รวมไปถึง อ่างทำความร้อน ขวดฟองไอน้ำ หัวต่อ และตัวควบแน่น |
| ศตวรรษที่ 17 และ 18 | ความสนใจนั้นมุ่งเน้นไปที่การพัฒนาเทคโนโลยีการกลั่นที่มีอยู่ให้ดียิ่งขึ้น มีการหุ้มฉนวนอุปกรณ์ในการกลั่น ชุดเครื่องมือต่างๆ ทำมาจากแก้วแทนการใช้โลหะ เริ่มมีใช้วิธีการกลั่นแบบต่อเนื่อง และใช้น้ำเป็นตัวหล่อเย็น อีกทั้งยังมีการค้นพบขั้นตอนการกลั่นระเหยในช่วงเวลานี้ด้วยเช่นกัน เมื่อช่วงปลายศตวรรษที่ 17 นักฟิสิกส์ชาวไอร์แลนด์ที่ชื่อว่า Robert Boyle (1627-1691) ได้ทำการกลั่นแบบสูญญากาศเป็นครั้งแรก |
| ศตวรรษที่ 19 | มีการประดิษฐ์คอลัมน์ตั้งฉากเป็นครั้งแรกเพื่อการกลั่นหลายชั้นได้สำเร็จ เมื่อเริ่มเข้าสู่ยุคของเคมีอินทรีย์ ได้มีการออกแบบอุปกรณ์เครื่องมือการกลั่นขึ้นใหม่ให้เข้ากับความต้องการใช้งานของห้องปฏิบัติการโดยเฉพาะ เมื่อมีเรื่องทางการเงินของอุตสาหกรรมแอลกอฮอล์ในฝรั่งเศสเข้ามาเกี่ยวข้อง จึงทำให้มีการพัฒนาเพื่อนำมาใช้ในอุตสาหกรรมขนาดใหญ่ได้อย่างรวดเร็วเช่นกัน การคิดค้นตัวปรับแรงดันและการพัฒนาปั้มต่างๆ ช่วยทำให้สามารถใช้งานระบบสูญญากาศได้มากขึ้น |
| 1950 - 1955 | บทความโดย C.C. Draig (1950) และ M.E. Volk (1955) ได้เผยแพร่หลักการทำงานเบื้องหลังการทำระเหยแบบหมุน กระบวนการนี้มีอัตราการถ่ายเทความร้อนที่ดียิ่งขึ้นกว่ากระบวนการที่ใช้ขวดแก้ว ซึ่งช่วยเก็บผลิตภัณฑ์และเพิ่มกำลังการผลิตได้มากขึ้น |
| 1957 | BÜCHI Labortechnik ใน Flawil ได้นำเครื่องทำระเหยแบบหมุนตัวแรกออกสู่ตลาด |
ขั้นตอนการกลั่นและเทคโนโลยีการทำระเหยแบบหมุนที่เกี่ยวข้อง
เครื่องทำระเหยแบบหมุนสร้างขึ้นเพื่อตอบสนองต่อความต้องการของนักเคมีและนักชีววิทยาทั่วโลก ด้วยคอนเดนเซอร์ที่หลากหลาย ทำให้สามารถนำ Rotavapor® มาใช้เพื่อการกลั่นสารละลายผสมได้อย่างรวดเร็ว ทำให้ตัวอย่างแห้งได้อย่างมีประสทธิภาพ เตรียมตัวอย่างแช่เยือกแข็งได้ไวยิ่งขึ้น สังเคราะห์สารเคมีภายใต้ภาวะการกลั่นรีฟลักซ์ สกัดแยกสารประกอบธรรมชาติและทำให้เข้มข้นได้ ตัวทำระเหยแบบหมุนสามารถนำไปใช้งานในอุตสาหกรรมได้หลากหลายนับไม่ถ้วน และยังรวมไปถึงกระบวนการเกี่ยวกับน้ำมันดิบ การแยกสารคานาบินอยด์ การทำอาหารโมเลกุลาร์ การสร้างสรรค์กลิ่นและรสชาติ รวมถึงอื่นๆ อีกมากมาย
การระเหยในขั้นตอนการกลั่น
การระเหยคือการเปลี่ยนอนุภาคจากสภาวะของเหลวเป็นสภาวะก๊าซ กระบวนการระเหยจะเริ่มต้นทันทีที่เงื่อนไขอุณหภูมิและแรงดันไปถึงกราฟจุดเดือด ที่จุดนี้ อนุภาคทั้งหมดจะมีพลังงานจลน์เพียงพอ ซึ่งนับเป็นพลังงานที่จำเป็นในการเอาชนะแรงพันธะยึดเกาะระหว่างอนุภาคด้วยกันไว้ จึงไม่ต้องสงสัยอีกต่อไปว่าโมเลกุลบางส่วนบนผิวหน้าสามารถแตกพันธะออกจากสถานะของเหลวได้อย่างไร การเปลี่ยนสภาวะของเหลวเป็นก๊าซจะเกิดขึ้นกับของเหลวทั้งหมด จุดเดือดคือสิ่งสำคัญในกระบวนการกลั่นเนื่องจากของเหลวนั้นระเหยเร็วมากกว่าในระหว่างการระเหย เนื่องจากปริมาตรต่อโมลของก๊าซมีมากกว่าของเหลวหลายเท่า ทำให้ตัวสารขยายออก 1,000- ถึง 2,000 เท่าในระหว่างการทำให้เดือด ต้องใช้ความระมัดระวังเพื่อให้แน่ใจว่าอุปกรณ์การกลั่นสามารถรองรับปริมาตรดังกล่าวนี้ได้
สภาวะนิวคลิเอตในระหว่างขั้นตอนการทำให้ระเหย
ขั้นตอนแรกในการเดือดระหว่างขั้นตอนการกลั่นคือสภาวะนิวคลิเอต ความร้อนทำให้ฟองก๊าซที่หุ้มอยู่ในผนังภาชนะเริ่มขยายตัว อนุภาคที่ระเหยจะทิ้งของเหลวไว้แล้วลอยไปกับฟองที่เกิดจนเพิ่มจำนวนขึ้น เมื่อฟองถึงจุดที่แรงลอยตัวเหนือกว่าแรงตึงผิวยึดเกาะได้ จะเกิดการแตกตัวบางส่วนออกจากผนังภาชนะและลอยสู่ผิวน้ำ ส่วนที่เหลือของฟองจะทำหน้าที่เป็นหัวเชื้อให้ฟองถัดไปในจุดเดียวกัน กระแสที่ลอยไหลขึ้นจะก่อตัวตามหลังฟอง ช่วยในการผสมกันภายในของเหลวมากขึ้น เมื่อของเหลวอุณหภูมิสูงขึ้น จะมีฟองก่อตัวมากขึ้นเรื่อยๆ จนกระทั่งมีชั้นไอระเหยปกคลุมรอบผนังภาชนะ ขั้นตอนนี้จะเกิดการเดือดแบบฟิล์ม
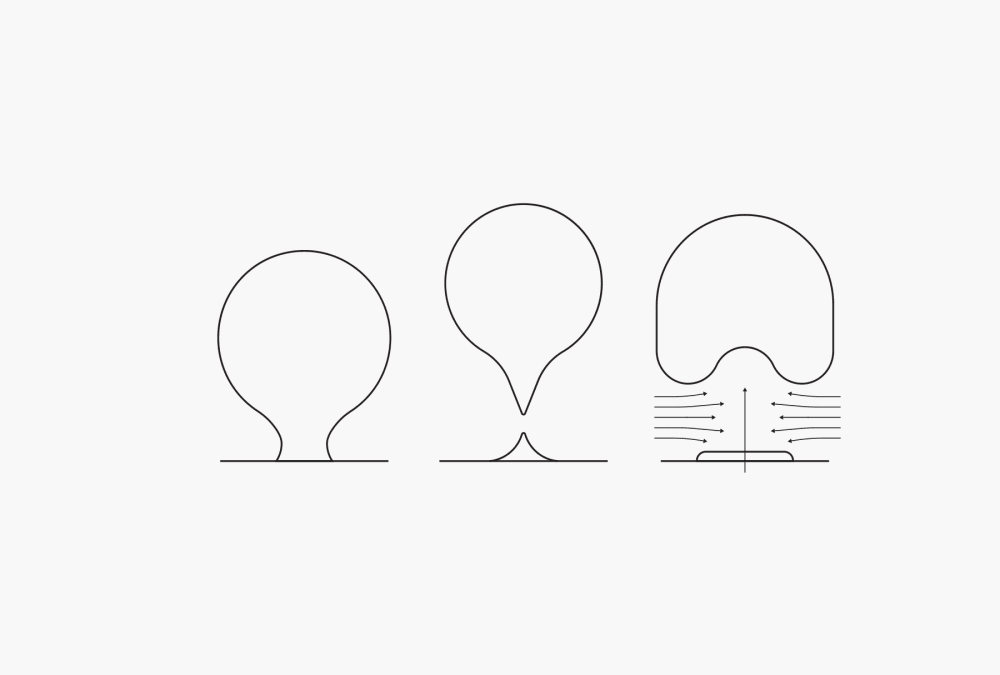
ภาพที่ 1 สภาวะนิวคลิเอต
ถ่ายเทความร้อนในระหว่างขั้นตอนการระเหยเป็นไอ
หนึ่งในสิ่งสำคัญของการเดือดคือการถ่ายเทความร้อนจากแหล่งกำเนิดความร้อนไปสู่ของเหลว เนื่องจากของเหลวมักจะสัมผัสกับแหล่งความร้อนเฉพาะบริเวณผนังของภาชนะ และชั้นนอกจะมีอุณหภูมิสูงขึ้นก่อน โดยชั้นบนสุดจะยังคงมีอุณหภูมิต่ำกว่า ชั้นที่อุ่นกว่าจะลอยสูงขึ้นตามการพาความร้อน และชั้นที่เย็นกว่าจะลงมาแทนที่ ทำให้เกิดการปรับอุณหภูมิให้เสมอกันได้แต่เป็นไปอย่างช้ามาก การคนผสมเพิ่มเติมในตอนเริ่มต้นของสภาวะนิวคลิเอตจะช่วยให้มีการถ่ายเทความร้อนได้ดียิ่งขึ้น แต่สภาวะที่ได้นั้นยังไม่เป็นที่น่าพอใจนัก สามารถเพิ่มการถ่ายเทความร้อนได้อย่างชัดเจนด้วยการทำให้ของเหลวเคลื่อนไหวด้วยตัวผสมหรือในขวดแบบหมุนโดยใช้เทคโนโลยีการทำระเหยแบบหมุน การผสมต่อเนื่องหรือการบังคับนำพาความร้อนช่วยให้มีการถ่ายเทความร้อนได้ดียิ่งขึ้น ขับอนุภาคสู่สภาวะก๊าซได้ดียิ่งขึ้น ดังนั้นจึงเร่งกระบวนการกลั่นให้เกิดขึ้นได้ไวยิ่งขึ้นเช่นกัน

ภาพที่ 2 การพาความร้อนแบบอิสระ
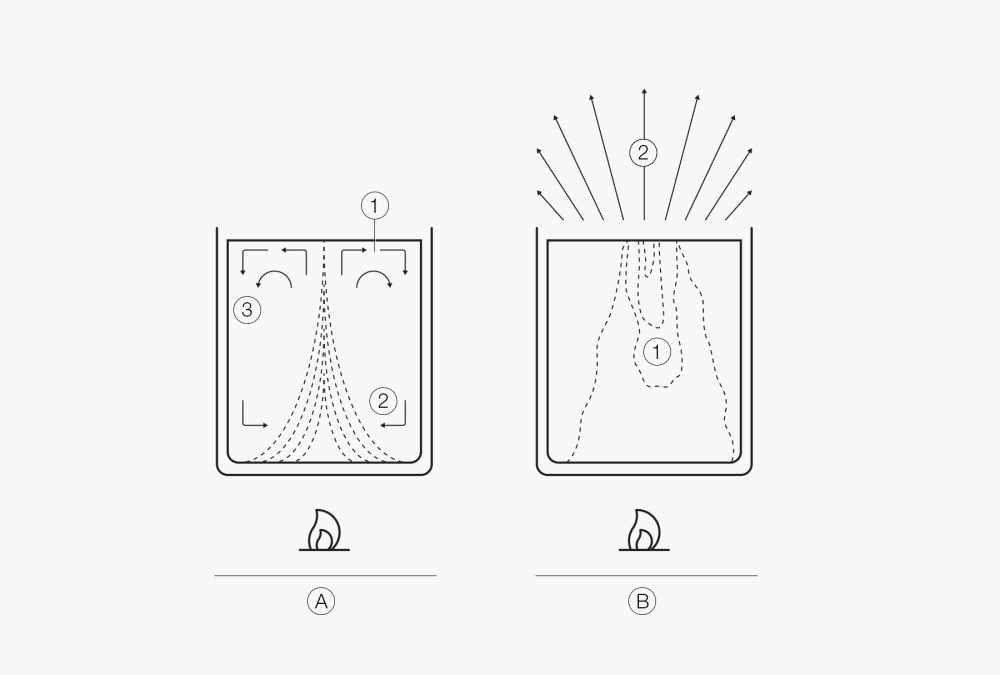
ภาพที่ 3:
เริ่มการเดือดแบบหน่วง (1. การชนกัน), (2. อุณหภูมิ โปรไฟล์ 3 การพาความร้อน)
การเดือดแบบหน่วง (1. การชนกัน) ที่พื้นผิว
การควบแน่นในขั้นตอนการกลั่น
การควบแน่นคือการย้อนกลับกระบวนการเดือดที่สารจะเปลี่ยนสถานะจากก๊าซเป็นของเหลว เมื่อต้องนำความร้อนในการทำระเหยถ่ายเทไปสู่อนุภาคในระหว่างการทำให้เดือดออกจากอนุภาค จำเป็นต้องใช้การทำให้เย็นเพื่อควบแน่นก๊าซ
ไอระเหยจะออกจากจุดระเหยไปสู่ส่วนของการควบแน่น เนื่องจากอุณหภูมิของคอนเดนเซอร์ต่ำกว่าอุณหภูมิควบแน่นของไอระเหย จึงเกิดการเร่งไอระเหยออกและชั้นฟิล์มของเหลวก่อตัวขึ้นทันทีที่โมเลกุลไปสัมผัสกับคอนเดนเซอร์ เนื่องจากชั้นฟิล์มนี้จะไปขัดขวางการถ่ายเทความร้อน จึงต้องมีการดำเนินการเพื่อให้แน่ใจว่าอนุภาคจะสามารถขับออกไปได้ คอนเดนเซอร์จึงมีการออกแบบให้เป็นแนวตั้งหรือแนวทแยงเสมอ อนุภาคที่ควบแน่นจึงไหลไปเก็บอยู่ในขวดเก็บ เนื่องจากปริมาตรของก๊าซที่จะควบแน่นนั้นมากกว่าของเหลวที่เกิดขึ้นอย่างชัดเจน จึงไม่สามารถนำพาความร้อนได้อย่างง่ายดายนัก จึงเป็นเหตุผลที่คูลเลอร์มักจะมีพื้นที่ผิวขนาดใหญ่มาก
เพื่อให้แน่ใจว่าคุณสามารถควบแน่นอนุภาคได้อย่างมีประสิทธิภาพตลอดกระบวนการกลั่นทั้งหมด จึงมีการใช้สื่อกลางระบายความร้อนที่สามารถหมุนเวียนได้อย่างต่อเนื่อง เช่น น้ำประปาไหลผ่านหรือใช้ตัวทำความเย็นแบบหมุนเวียนได้ การทำให้เดือดส่งผลให้แรงดันเพิ่มสูงขึ้นอย่างมาก ในการควบแน่น ปัญหาแรงดันที่มหาศาลจะค่อยๆ ลดลง ซึ่งตัวคอนเดนเซอร์นั้นทำหน้าที่เหมือนเป็นตัวปั๊ม
วิธีส่งผ่านก๊าซในตัวทำระเหยแบบหมุน
การกลั่นประกอบด้วย การทำระเหยและการควบแน่นในภายหลังเนื่องจากจุดที่เกิดการระเหย และควบแน่นนั้น แยกจากกันอย่างชัดเจน จึงต้องมีการนำพาเคลื่อนย้ายไอระเหย ซึ่งสามารถทำได้อย่างง่ายดาย เนื่องจากก๊าซสามารถกระจายตัวเองได้อย่างทั่วถึงในพื้นที่ว่างที่มี จึงเกิดการไหลจากฝั่งตัวทำระเหยไปยังฝั่งคอนเดนเซอร์ได้ เมื่อมีการทำให้เป็นของเหลว ซึ่งทำให้เกิดเป็นหยดปริมาตรที่เทียบเท่ากัน แล้วจึงเกิดภาวะสูญญากาศในระบบขึ้น ฝั่งคอนเดนเซอร์จะดึงเอาก๊าซเข้ามา ขณะที่ฝั่งตัวทำระเหยจะจ่ายก๊าซออกมาในปริมาณที่เท่ากัน ไดนามิกความแตกต่างของแรงดันจึงสร้างการเคลื่อนไอระเหยผ่านชุดเครื่องมือด้วยความเร็วสูง แรงที่รักษาการไหลนี้คือความร้อนของการระเหยที่จ่ายให้กับก๊าซในระหว่างการทำระเหย และความร้อนดังกล่าวจะถูกดึงออกในระหว่างการควบแน่น ปรากฏการณ์นี้จึงเรียกว่าเป็นการทำเทอร์มอลปั๊ม (Thermal Pump - P)
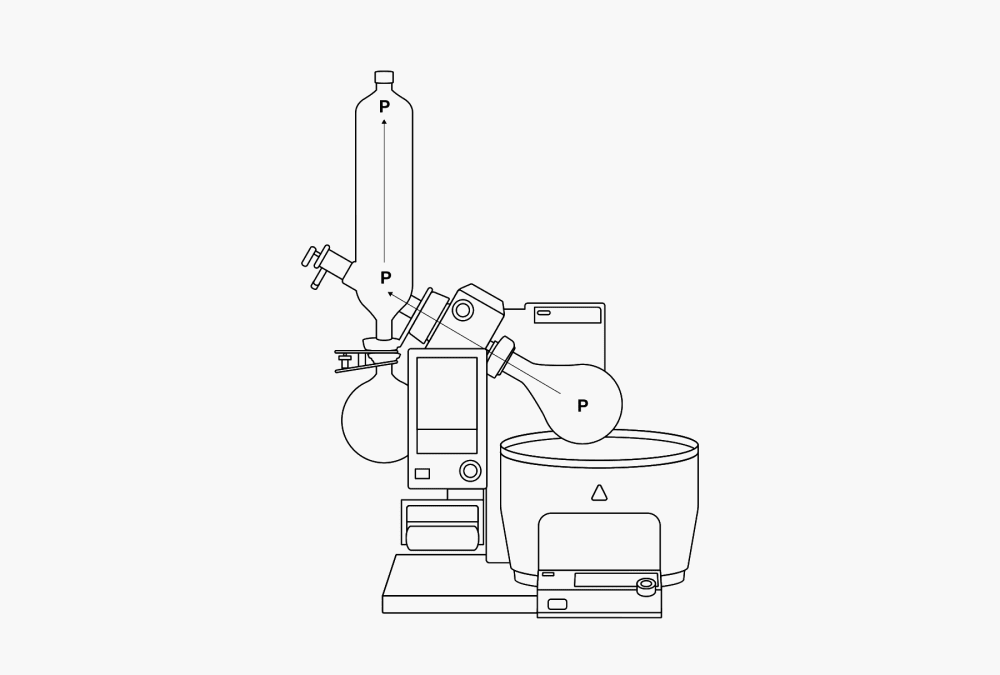
ภาพที่ 4 เทอร์มอลปั๊ม (P) และความแตกต่างของอุณหภูมิในระบบภายในตัวทำระเหยแบบหมุน
เพื่อรักษาสมดุลความต่างของแรงดันไดนามิก สิ่งสำคัญคือ ต้องปรับความเร็วของการควบแน่น และความเร็วในการระเหยให้เข้ากัน เมื่อใดที่มีสารเกิดการระเหยมากกว่าที่ควบแน่นได้ในคอนเดนเซอร์ แรงดันภายในชุดอุปกรณ์จะเพิ่งสูงขึ้นและปั๊มสูญญากาศจะต้องดึงตัวทำละลายอย่างต่อเนื่องแล้วปั๊มออกสู่สิ่งแวดล้อม จุดที่เหมาะสมคือการให้อุณหภูมิต้มเดือดสูงกว่าอุณหภูมิของน้ำหล่อเย็นประมาณ 20 °C การกำหนดอุณหภูมินี้ช่วยให้แน่ใจได้ว่าสามารถรักษาดุลยภาพของความร้อนได้
การแยกด้วยกระบวนการกลั่น
การกลั่นเป็นเทคนิคการแยกสำหรับการแยกสารผสมที่เกิดจากของเหลวสองชนิด กระบวนการกลั่น จะขึ้นอยู่กับความแตกต่างระหว่างแรงดันไอของสารต่างๆ สารผสมจะได้รับความร้อน จนกระทั่งระเหยและควบแน่นกลับมาอีกครั้ง ในขั้นตอนนี้ องค์ประกอบที่กลายเป็นไอได้ง่ายกว่า จะสะสมในไอระเหย แล้วจึงควบแน่นเกิดเป็นการแยกขึ้นได้ ไอระเหยที่เพิ่มขึ้น ผ่านอุปกรณ์การกลั่นไปถึงยังคอนเดนเซอร์ที่ไหลไปรวมในท่อเก็บ เป็นสารที่ได้จากการกลั่น ขณะเดียวกันองค์ประกอบที่ระเหยเป็นไอได้ยากกว่าจะสะสมอยู่ในขวดระเหย
หากจุดเดือดของสารทั้งสองต่างกันเกินกว่า 80 °C ก็จะสามารถแยกสารผสมได้ด้วยการกลั่นเพียงครั้งเดียว โดยหลักแล้วจะใช้การกลั่นเพียงครั้งเดียวเพื่อแยกตัวทำละลายที่ระเหยเป็นไอได้ง่ายจากวัสดุที่มีจุดเดือดสูง ทำให้ไม่มีความแตกต่างว่าจะได้ตัวทำละลาย (การทำความสะอาดตัวทำละลาย) หรือสิ่งตกค้าง (การทำความสะอาดผลิตภัณฑ์ของปฏิกิริยาด้วยการแยกตัวทำละลายออก) กลับมาใหม่หรือไม่ เมื่อจุดเดือดขององค์ประกอบทั้งสองที่จะแยกนั้นใกล้กันมากเกินไป จะต้องทำซ้ำกระบวนการกลั่นหลายครั้งมากขึ้น ซึ่งกระบวนการนี้เรียกว่าการทำให้บริสุทธิ์ด้วยการกลั่นซ้ำ (Rectification) หรืออีกวิธีหนึ่ง สามารถใช้การกลั่นลำดับส่วน (Fractional Distillation) เพื่อแยกของเหลวสองชนิดที่มีอุณหภูมิจุดเดือดต่างกันไม่มากได้ ในการกลั่นลำดับส่วน คอลัมน์ลำดับจะมีลูกแก้วหรือเม็ดพลาสติกใส่ไว้ระหว่างขวดต้มเดือดและคอนเดนเซอร์ ลูกแก้วในคอลัมน์ลำดับจะเพิ่มพื้นผิวสัมผัสให้ของเหลวสามารถควบแน่น ระเหยซ้ำ แล้วจึงควบแน่นอีกครั้งได้
หน้าที่ของภาวะสูญญากาศในกระบวนการกลั่น
ภาวะสูญญากาศมีบทบาทสำคัญกับตัวทำระเหยทุกประเภทเนื่องจากจะช่วยลดอุณหภูมิจุดเดือดที่จำเป็นสำหรับการกลั่นลงได้ ซึ่งอาจควบคุมภาวะสุญญากาศได้เอง หรืออัตโนมัติได้เช่นกัน หากมีการติดตั้งตัวควบคุมภาวะสูญญากาศ (Vacuum Controller) ภาวะสุญญากาศจะก่อตัวขึ้น ในแหล่งกำเนิดสูญญากาศนอกตัวทำระเหยแบบหมุน ซึ่งอาจเป็นปั๊มในห้องปฏิบัติการ ไม่ว่าจะเป็นปั๊มหัวฉีดน้ำ หรือปั๊มไดอะแฟรม หรือแม้แต่ท่อสูญญาณกาศในตัวระบบเองก็ตาม การทำงานของปั๊มห้องปฏิบัติการสามารถปรับควบคุมได้ด้วยตัวควบคุมภาวะสูญญากาศที่ช่วยประหยัดน้ำ ประหยัดไฟ และยืดอายุการใช้งานของปั๊มได้
Rotavapor® จะเติมอากาศเข้าและดูดอากาศออก ณ ข้อต่อสุญญากาศต่างๆในชุดอุปกรณ์แก้ว ซึ่งตำแหน่งของข้อต่อนี้ ถือว่ามีความสำคัญเพราะต้องอยู่ในตำแหน่งที่มีการลดระดับแรงดันเกินในระบบสะสมจากการระเหยลงด้วยการควบแน่นซึ่งจะเกิดขึ้นที่จุดสูงสุดของสารทำความเย็นขาเข้า และจุดล่างสุดของสารทำความเย็นขาออก

